Atomistique et classification périodique
1. Noyau, isotopie et électrons
1.1 Définition du noyau
Le noyau est constitué de protons et de neutrons, aussi appelés nucléons. Les protons sont chargés positivement, tandis que les neutrons sont neutres. La force de liaison nucléaire assure la cohésion du noyau malgré la répulsion entre protons.
Définition
Un atome est constitué d’un noyau central très dense autour duquel « gravitent » des électrons chargés négativement.
1.2 Isotopie
L’isotopie est le phénomène par lequel des atomes d’un même élément possèdent le même nombre de protons (donc le même numéro atomique) mais un nombre différent de neutrons. Par exemple, les isotopes de l’hydrogène sont le protium (1H), le deutérium (2H) et le tritium (3H).
1.3 Électrons
Les électrons sont des particules subatomiques de charge négative gravitant autour du noyau. Leur distribution autour du noyau définit les propriétés chimiques de l’atome.
1.4 Masse du proton et de l’électron
- Masse du proton : \( m_p = 1.672 \times 10^{-27} \) kg
- Masse de l’électron : \( m_e = 9.109 \times 10^{-31} \) kg
Les protons sont environ 1800 fois plus massifs que les électrons.
Exercices corrigés
Exercice 1 : Quel est le nombre de neutrons dans l’isotope \( ^4He \) ?
Correction : Le nombre de neutrons est \( A – Z = 4 – 2 = 2 \).
Exercice 2 : Calculez la différence de masse entre un proton et un électron.
Correction : \( \Delta m = m_p – m_e = 1.672 \times 10^{-27} – 9.109 \times 10^{-31} \approx 1.672 \times 10^{-27} \) kg.
Exercice 3 : Combien d’électrons possède un atome de carbone neutre ?
Correction : Le carbone a un numéro atomique \( Z = 6 \), donc il possède 6 électrons.
2. Fonction d’onde et équation de Schrödinger
2.1 Fonction d’onde
La fonction d’onde, notée \( \psi(r, t) \), est une fonction complexe qui nous sert à décrire les particules de petite taille comme par exemple les électrons. Elle ne correspond pas directement à une grandeur physique mesurable. Cependant, le carré de son module, \( |\psi(r, t)|^2 \), représente la densité de probabilité de présence de la particule dans une région donnée de l’espace à un instant précis.
Définition
Les fonctions d’onde \( \psi(r, t) \) sont les solutions de l’équation de Schrödinger, et \( |\psi(r, t)|^2 \) donne la probabilité de présence d’un électron dans une région de l’espace.
La probabilité \( P \) de trouver un électron dans une région d’espace \( d\tau \) est donnée par :
\( P = \int_V |\psi(r, t)|^2 d\tau \)
2.2 L’équation de Schrödinger
2.2.1 Équation de Schrödinger indépendante du temps
L’équation de Schrödinger pour les systèmes stationnaires s’écrit :
\( \hat{H}\psi(r) = E\psi(r) \)
2.2.2 L’opérateur Hamiltonien
L’opérateur Hamiltonien, noté \( \hat{H} \), représente l’énergie totale du système et se décompose en énergie cinétique et potentielle :
\( \hat{H} = \hat{T} + \hat{V} \)
2.3 Les orbitales atomiques
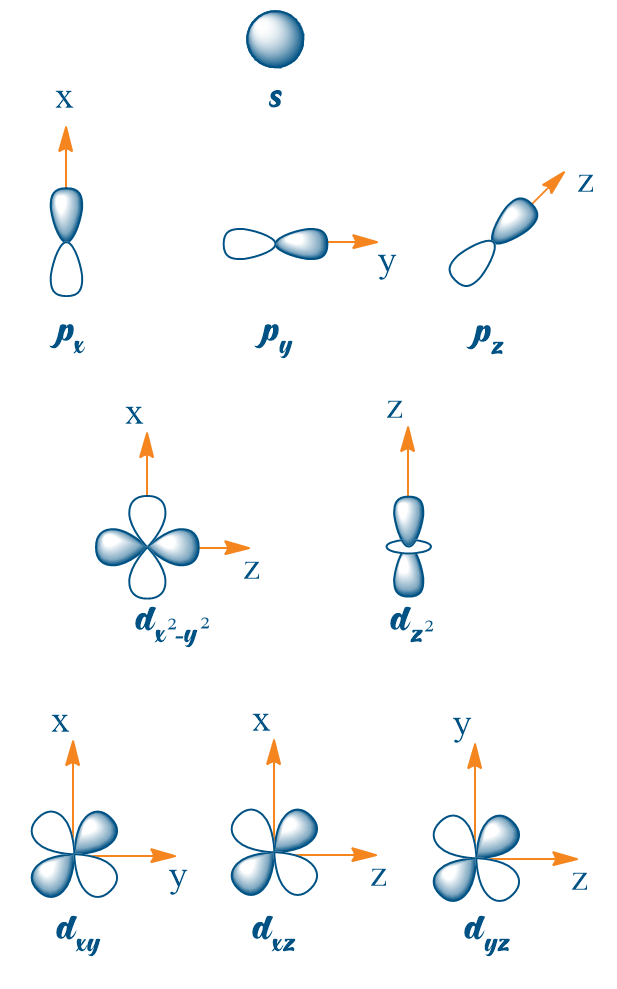
Les orbitales atomiques indiquent les volumes où les électrons ont les plus fortes probabilités de présence. Elles ont différentes formes : sphériques (s), à double lobe (p), et plus complexes (d).
2.4 Les nombres quantiques
Il existe quatre nombres quantiques pour caractériser chaque électron dans un atome :
- n : nombre quantique principal, indique la couche électronique.
- l : nombre quantique azimutal, détermine la forme de l’orbitale.
- ml : nombre quantique magnétique, détermine l’orientation de l’orbitale.
- ms : nombre quantique de spin, caractérise le spin de l’électron.
Conseil
Le nombre \( l \) peut prendre des valeurs allant de 0 à \( n-1 \). Par exemple, pour \( n = 3 \), \( l \) peut être 0, 1 ou 2.
Les valeurs possibles de \( ml \) varient de \(-l\) à \(+l\). Le nombre \( ms \) peut être \( \pm \frac{1}{2} \).
3. Atome monoélectronique, atomes polyélectroniques et configuration électronique
3.1 Atome monoélectronique
Un atome monoélectronique est un atome qui ne possède qu’un seul électron dans son cortège électronique. Un exemple classique d’atome monoélectronique est l’atome d’hydrogène. Ces atomes sont plus simples à étudier du point de vue théorique, car leur unique électron interagit directement avec le noyau sans être influencé par la présence d’autres électrons.
Ce type d’atome est souvent utilisé dans les modèles quantiques simplifiés pour illustrer des concepts fondamentaux de la chimie et de la physique atomique, tels que les orbitales atomiques ou la quantification de l’énergie.
Les atomes monoélectroniques incluent également des ions hydrogénoïdes, qui sont des ions contenant un seul électron autour d’un noyau ayant une charge supérieure à celle de l’hydrogène, comme les ions He+ ou Li2+.
3.2 Atomes polyélectroniques
Les atomes polyélectroniques possèdent plusieurs électrons, qui interagissent entre eux. Leur configuration électronique est déterminée par les principes de Pauli et de Hund.
3.3 Configuration électronique
La configuration électronique d’un atome décrit la répartition de ses électrons dans les orbitales atomiques. Par exemple, la configuration électronique de l’oxygène (Z = 8) est : 1s2 2s2 2p4.
Formule
Principe de Pauli : deux électrons ne peuvent pas avoir les mêmes quatre nombres quantiques dans un même atome.
Règle de Hund : les électrons occupent un maximum d’orbitales de même énergie avant de se coupler. Les électrons non appariés sont de même spin.
3.4 Électrons de cœur et électrons de valence
Les électrons de cœur sont ceux des couches internes, tandis que les électrons de valence sont ceux des couches les plus externes, qui participent aux liaisons chimiques.
Exercices corrigés
Exercice 1 : Donnez la configuration électronique du fer (Z = 26).
Correction : 1s2 2s2 2p6 3s2 3p6 4s2 3d6.
Exercice 2 : Identifiez les électrons de valence du chlore (Z = 17).
Correction : Les électrons de valence sont ceux de la couche 3p : 3s2 3p5.
Exercice 3 : Appliquez le principe de Pauli à la configuration électronique du soufre (Z = 16).
Correction : Aucun électron n’a les mêmes quatre nombres quantiques.
4. Classification périodique des éléments
4.1 Construction du tableau périodique
Le tableau périodique classe les éléments en fonction de leur numéro atomique croissant. Les éléments d’une même colonne possèdent des propriétés chimiques similaires car ils ont la même configuration électronique de valence.
4.2 Rayon atomique et électronégativité
Le rayon atomique diminue de gauche à droite dans une période et augmente de haut en bas dans une colonne. L’électronégativité, qui mesure la capacité d’un atome à attirer les électrons, suit la tendance inverse.
4.3 Évolution de l’affinité électronique et de l’énergie d’ionisation
L’affinité électronique et l’énergie d’ionisation augmentent de gauche à droite dans une période et diminuent de haut en bas dans une colonne.
Exercices corrigés
Exercice 1 : Classez les éléments suivants par ordre croissant d’énergie d’ionisation : Na, Cl, Mg.
Correction : Na < Mg < Cl
Exercice 2 : Expliquez la variation du rayon atomique entre le lithium et le fluor.
Correction : Le rayon atomique diminue car la charge nucléaire effective augmente, attirant les électrons plus près du noyau.
Exercice 3 : Donnez l’évolution de l’électronégativité dans une période.
Correction : L’électronégativité augmente de gauche à droite dans une période.
